Im Rahmen des Verbundprojekts SynergyFuels, sind 3 Professuren am TUM-Campus Straubing für die nachhaltige Formaldehydsynthese zuständig: Professur für Chemische-und Thermische Verfahrenstechnck (TUM CTV), Lehrstuhl für Chemie Biogener Rohstoffe (TUM CBR), und Professur Elektrobiotechnologie (TUM EBT).
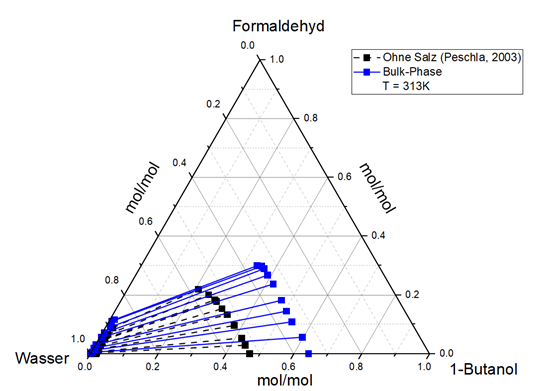
Um den Prozess der Formaldehydsynthese und die Produktion von Ausgangsstoffen für die OMBE-Synthese zu konzeptualisieren, wurden zunächst von TUM CTV mehrere Experimente durchgeführt, um die Dampf-Flüssigkeit- und Flüssig-Flüssig-Gleichgewichte des Prozessgemischs zu messen. Da die Prozessmedien Salze und Puffersubstanzen enthielten, wurde auch deren Einfluss auf die Gleichgewichte gemessen. Da die vorhandene Apparatur ungenau war, wurde eine neue Apparatur maßgefertigt, um den Salzeffekt auf das Dampf-Flüssigkeit-Gleichgewicht zu erfassen.
Zudem wurde ein Aktivitätsmodell entwickelt, um das Verhalten des Prozessgemischs zu beschreiben. Dieses Modell wird künftig verwendet werden, um verschiedene nachgelagerte Prozesse zu simulieren und ihre Durchführbarkeit zu bewerten, u.a. die Destillation und Flüssig-Flüssig-Extraktion. Zusätzlich wurde eine Auswahl verschiedener Adsorptionsmittel identifiziert. Für die Zukunft sind Experimente geplant, mit denen die Durchführbarkeit der Einbindung eines Adsorptionsprozesses ermittelt werden soll.

Um die Formaldehydsynthese aus Methanol nachhaltiger zu gestalten, wurden bei TUM CBR und TUM EBT Enzyme aus drei Unterklassen – Dehydrogenasen (NAD(P)+– oder PQQ-abhängig) und Oxidasen (FAD-abhängig, sauerstoffabhängig) – untersucht. Mehr als 40 Enzymkandidaten wurden hinsichtlich ihrer Methanolaktivität getestet. Die Expression von Oxidasen (aus Eukaryoten) und PQQ-abhängigen Dehydrogenasen (aus Methanotrophen) in prokaryotischen Zellen war aufwendig, gelang aber erstmals für zwei eukaryotische Oxidasen.
Rund 20 aktive Kandidaten wurden hinsichtlich ihrer Methanolaffinität, Aktivität, Stabilität und Überoxidation charakterisiert. NAD-abhängige Dehydrogenasen zeigten eine geringe Methanolaffinität und -Aktivität sowie minimale Überoxidation. Sie zeigten eine moderate Toleranz gegenüber Methanol und eine geringe Toleranz gegenüber Formaldehyd, was angesichts der Reaktivität nicht überraschend ist. Oxidasen zeigten eine hohe Methanolaktivität und -affinität, jedoch auch eine signifikante Formaldehydüberoxidation. PQQ-abhängige Dehydrogenasen bevorzugten Ethanol und verhielten sich bezüglich Methanol ähnlich wie NAD-abhängige Dehydrogenasen.
Die Vertreter jeder Enzymunterklasse wurden im elektrochemischen Reaktor mit unterschiedlichen Elektronenmediatoren gekoppelt. Nach der Optimierung, basierend auf der besten Mediator-Enzym-Kombination, wird der bevorzugte Enzymkandidat für künftiges Engineering ausgewählt werden. Während aktuell an Hochdurchsatz-Screening-Verfahren und der Integration des elektrochemischen Reaktors gearbeitet wird, sind zudem rationale Strategien für Enzym-Engineering und Ansätze zur Immobilisierung geplant.
